(1)某学生在实验室做了5个实验
①在铝盐溶液中逐滴加入稀氨水直至过量, ②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量, ④在偏铝酸钠溶液中通入CO2直至过量, ⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下 * * 种图象(纵坐标为沉淀物质的量,横坐标为溶液中加入物质的量)实验与图象对立关系正确的是:___________。
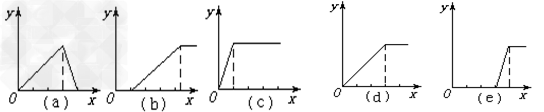
(2)已知:氧化性:KMnO4>HNO3;Bi位于周期表中VA,+3价较稳定,NaBiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__________________________;
(b)实验④中的现象为:_____________________________;
(c)实验②反应的离子方程式是:_____________________。
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
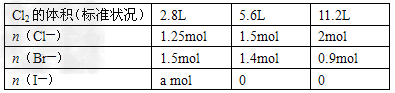
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方_________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为:________________ 。
(1 )CD
(2 )(a )PbO2>KMnO4>H2O2;(b )紫红色褪去,生成白色沉淀;(c )2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2
(3 )①Cl2+2I-==I2+2Cl- ;②10:15:4
