问题
问答题
氯化镁是制取镁的原料之一.现要测定某化工产品(含MgCl2和KCl)中所含的氯化镁质量分数,进行实验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充分振荡,实验所得数据见下表:
| 编号 | 1 | 2 | 3 | 4 | 5 |
| 加入氢氧化钾溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
| 生成沉淀的质量/g | 0.58 | a | 1.74 | 2.32 | 2.32 |
(1)表中a为______.
(2)样品中的氯化钾属于化肥中的______肥,可回收利用.
(3)所用的氢氧化钾溶液中溶质的质量分数是______.
(4)计算样品中氯化镁的质量分数是多少?(写出计算过程)
答案
(1)由表中1、3两次的数据可知,10g氢氧化钾溶液与氯化镁反应能生成0.58g沉淀,因此20g氢氧化钠溶液能生成1.16g沉淀.
(2)氯化钾提供的主要营养元素是钾元素,属于钾肥.
(3)设10g氢氧化钾溶液中溶质氢氧化钾的质量为x.
MgCl2+2KOH═2KCl+Mg(OH)2↓
112 58
X 0.58克
=112 X 58 0.58g
X=1.12g
氢氧化钾溶液中溶质的质量分数为:
×100%═11.2%1.12g 10g
答:氢氧化钾溶液中溶质的质量分数为11.2%
(4)设原混合物中含有MgCl2的质量为x.
MgCl2+2KOH=Mg(OH)2↓+2KCl
95 58
x 2.32g
=95 58
,x=3.8g x 2.32g
则样品中氯化镁的质量分数是
×100%=38%3.8g 10g
答:样品中氯化镁的质量分数是38%

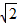 sinl00πt(V),则下列说法中正确的是( )
sinl00πt(V),则下列说法中正确的是( ) V
V