问题
选择题
关于下列图示的说法中正确的是( )
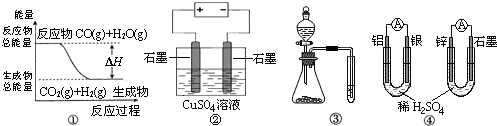
A.图①表示CO(g)+H2O(g)⇌CO2(g)+H2(g)是放热反应
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定为1:1
C.图③实验装置可一次而又科学准确的完成比较Cl2、Br2、I2单质氧化性强弱的实验
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
答案
A、根据能量守恒定律知,反应物的能量大于生成物的能量,该反应是放热反应,故A正确;
B、电解硫酸铜溶液时,阳极上生成氧气,阴极上析出铜单质,电解方程式为:2CuSO4+2H2O=2Cu+O2↑+2H2SO4由方程式知,铜和氧气的物质的量之比为2:1,故B错误;
C、氯气和溴都能置换出碘单质,所以不能一次而又科学准确的完成比较Cl2、Br2、I2单质氧化性强弱的实验,故C错误;
D、Al-Ag-H2SO4构成的原电池中负极上发生的电极反应式为Al-3e-=Al3+,Zn-石墨-H2SO4构成的原电池中负极上发生的电极反应式为Zn-2e-=Zn2+,因金属原子生成离子时失去的电子数不同,所以通过导线的电子数相同时,消耗负极材料的物质的量不同,故D错误;
故选A.
