背景材料:
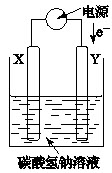
铝合金以质轻、稳定性好等优点广泛应用于航空航天事业。在铝合金表面能形成一层较厚的氧化膜,这是其在空气中稳定存在的关键。其反应原理是以铝件与另一种材料为电极,以某种溶液作电解质溶液进行电解,通电后在铝件与电解质溶液的接触面上逐渐形成一层氢氧化铝薄膜,薄膜的某些部位存在着小孔,电流从小孔中通过并产生热量使氢氧化铝分解,从而使铝件表面形成一层较厚的氧化膜。某校课外兴趣小组的同学根据上述原理,以铝件和铁棒为电极,以一定浓度的碳酸氢钠溶液为电解质溶液进行实验,实验装置如图所示。
问题:
(1)铝件放在()(填“X”或“Y”)极。
(2)铝件表面形成氢氧化铝的电极反应式是()。
(3)电解过程中,必须使电解质溶液的pH保持相对稳定(不能太大也不能太小)的原因是()。
(4)用碳酸氢钠溶液作电解质溶液,而不用碳酸钠溶液作电解质溶液,其理由是()。
参考答案:
(1)X
(2)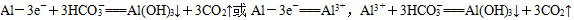
(3)氧化铝和氢氧化铝都是两性化合物,如果溶液的酸性或碱性过强,都会使所形成的氧化铝薄膜溶解
(4)碳酸氢钠的作用之一是中和阴极区溶液中过量的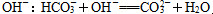
解析:
(1)要生成氢氧化铝,必须先生成铝离子,所以铝件应放在阳极,发生氧化反应,失电子变成阳离子。铁棒放在阴极。电子总是从电源的负极流出,所以装置中的Y极为阴(铁棒),X极(铝件)为阳极。
(2)碳酸氢钠溶液呈碱性,阳极发生反应: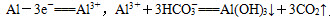 阴极发生反应:
阴极发生反应: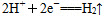
(3)要使铝件表面生成一层较厚的氧化膜,则不能使溶液溶解氧化铝和氢氧化铝,从氧化铝和氢氧化铝的两性角度考虑,必须使电解质溶液的pH保持相对稳定。
(4)等浓度碳酸氢钠溶液比碳酸钠溶液的碱性弱,有利于控制溶液的酸碱性。
