用惰性电极电解NaCl和CuSO4混合溶液250mL,经过一段时间后两极均得到11.2L气体(标准状况下),则下列有关描述中,正确的是()
A.阳极发生的电极反应只有:4OH--4e-===2H2O+O2↑
B.两极得到的气体均为混合物气体
C.若Cu2+的起始浓度为1mol/L,则c(Cl-)起始浓度为2mol/L
D.Cu2+的起始浓度最大应小于4mol/L
参考答案:C
解析:根据放电顺序,阴极放电顺序为:铜离子、氢离子,阳极放电顺序为氯离子、氢氧根离子,因此阳极可能生成氯气、氧气,而阴极只能生成氢气;若Cu2+的起始浓度为1mol/L,则阴极得到氢气11.2L时共转移的电子数为1.5mol,若Cl-起始浓度为2mol/L,则阳极得到氯气0.25mol、氧气0.25mol,阴极转移的电子总数也为1.5mol,符合电子守恒定律;由于阴极得到氢气,故Cu2+的起始浓度最大应小于2mol/L。

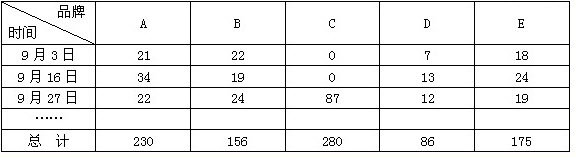
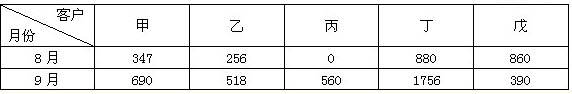 注:省烟草专卖局规定,卷烟零售户月订购卷烟数量超过上月量100%的,要提出预警,确定为异常订单。其中,零售户丙8月31日停业期满,于9月份恢复营业。 材料3 专卖部门查获了100条的飘雪牌真品卷烟,在抄条码时发现全部打了测试码。 材料4 收集了部分烟农合同约订面积与交售烟叶的数据:烟农甲约定8亩,交售了1578公斤烟叶,烟农乙约定10亩,交售了1983公斤烟叶,烟农丙约定11亩,交售了2301公斤烟叶。内管部门还接到了关于郁山烟叶收购站的工作人员李渔违规收购烟叶的举报。 请根据材料回答下列问题:
注:省烟草专卖局规定,卷烟零售户月订购卷烟数量超过上月量100%的,要提出预警,确定为异常订单。其中,零售户丙8月31日停业期满,于9月份恢复营业。 材料3 专卖部门查获了100条的飘雪牌真品卷烟,在抄条码时发现全部打了测试码。 材料4 收集了部分烟农合同约订面积与交售烟叶的数据:烟农甲约定8亩,交售了1578公斤烟叶,烟农乙约定10亩,交售了1983公斤烟叶,烟农丙约定11亩,交售了2301公斤烟叶。内管部门还接到了关于郁山烟叶收购站的工作人员李渔违规收购烟叶的举报。 请根据材料回答下列问题: