问题
选择题
下列图像表达正确的是 ( )
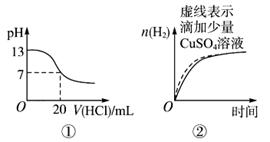
A.图①表示25 ℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水
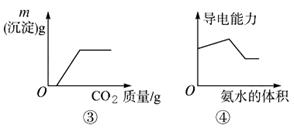
B.图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应
C.图③表示向CaCl2溶液中通入CO2
D.图④表示向醋酸溶液中滴入氨水
答案
答案:D
题目分析:A.因为氨水为弱碱,20mL 0.1mol/L氨水的PH小于13.
 B.Zn与HCl的反应方程式为Zn+2HCl
B.Zn与HCl的反应方程式为Zn+2HCl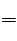 ZnCl2+H2 ,而CuSO4与Zn的反应方程式为
ZnCl2+H2 ,而CuSO4与Zn的反应方程式为
CuSO4+Zn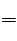 ZnSO4+Cu,生成的Cu并不能和HCl反应,故生成的氢气应该比没加硫酸铜的少。
ZnSO4+Cu,生成的Cu并不能和HCl反应,故生成的氢气应该比没加硫酸铜的少。
C.CO2加入到CaCl2溶液中,先生成CaCO3固体,故刚开始的质量不为0.
D.在醋酸中加入氨水,发生反应NH3+CH3COOH====CH3COONH4,NH3·H2O和CH3COOH是弱电解质而铵盐是强电解质,所以,导电能力增强。反应完全后,随着弱电解质氨水的加入,溶液被稀释,导电能力又下降,最后稳定但不为0。
点评:此题用图像的方法,考核了学生对弱酸弱碱反应对PH、导电能力等的掌握。
