问题
选择题
水的电离平衡为H2O 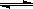 H+﹢OH-,△H>0,下列叙述不正确的是
H+﹢OH-,△H>0,下列叙述不正确的是
A.将水加热,pH减小
B.恒温下,向水中加入少量固体KOH,Kw不变
C.向水中滴入稀醋酸,c(H+)增大
D.向水中加入少量固体NaClO,平衡逆向移动
答案
答案:D
题目分析:因为水溶液电离平衡反应△H>0为吸热反应,A、将水加热后电离反应吸收热量,使反应正向进行,故A正确;B、Kw只与温度有关,与溶液浓度无关,因为表示反应在恒温下进行,故B正确;C、在水溶液中滴入醋酸后醋酸发生电离反应CH3COOH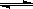 H++CH3COO-,c(H+)浓度增大,故C正确;D、 NaClO溶解放热,电离反应应正向移动,故D错误。
H++CH3COO-,c(H+)浓度增大,故C正确;D、 NaClO溶解放热,电离反应应正向移动,故D错误。
