为了比较卤素单质的氧化性强弱可在实验室先制取Cl2(利用MnO2与浓盐酸反应可制取Cl2)并将Cl2依次通入NaBr溶液和KI淀粉溶液中。如图所示仪器及药品试回答: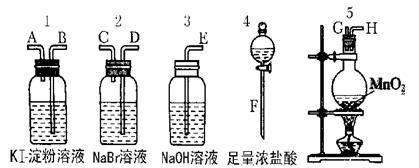
(1)若所制取气体从左向右流向时上述仪器接口的连接顺序为F接G、H接______、______接______、A接E。
(2)实验开始后装置5中反应的化学方程式为______________________。
(3)装置3的作用是________________________
反应的离子方程式为______________________________________。
(4)装置1中产生的现象是___________ 反应的离子方程式为____________________。
(5)若溴离子的还原性弱于碘离子的还原性,通过实验,卤素单质的氧化性由强到弱的顺序为__________________。
(共10分。第1小题1分,方程式2分每条,其余每空1分)
(1)H接D , C接B (2)MnO2 + 4HCl(浓)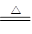 MnCl2 +Cl2↑+2H2O
MnCl2 +Cl2↑+2H2O
(3)吸收尾气,防止污染 Cl2 + 2OH- = Cl- + ClO- +H2O
(4)溶液变蓝 Cl2 + 2I-= I2 + 2Cl- (5)Cl2>Br2>I2
题目分析:(1)实验室用装置5制备氯气,经过1、2装置验证氯气的强氧化性,氯气有毒,不能直接排放到空气中,应用3装置吸收氯气,则各仪器从左至右的连接顺序为F接G、H接D , C接B、A接E。
(2)二氧化锰和浓盐酸反应的化学方程式是MnO2 + 4HCl(浓)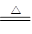 MnCl2 +Cl2↑+2H2O。
MnCl2 +Cl2↑+2H2O。
(3)氯气有毒,不能直接排放到空气中,应用3装置吸收氯气,防止污染,有关反应的离子方程式是Cl2 + 2OH- = Cl- + ClO- +H2O。
(4)氯气能和碘化钾发生置换反应生成碘单质,单质碘遇淀粉显蓝色,则实验现象是溶液变蓝 Cl2 + 2I-= I2 + 2Cl- 。
(5)根据非金属性较强的可以置换出减弱的可知,卤素单质的氧化性由强到弱的顺序为Cl2>Br2>I2。
点评:该题是高考中的常见题型,属于中等难度的试题,试题贴近高考,综合性强,有利于调动学生的学习兴趣,激发学生的学习积极性。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
