问题
填空题
(8分)实验室里迅速制备少量氯气可利用以下反应:
2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)用“线桥法”表示出电子转移情况:
2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
(2)该反应中,氧化剂是__________,还原剂是_________。
(3) 当电子转移的数目为6.02×1023个时生成的氯气的物质的量为 mol
答案
(8分)
(1) (2分)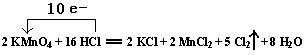 (单、双线桥皆可)
(单、双线桥皆可)
(2) (每空2分) KMnO4 ; HCl (3) (2分) 0.5
题目分析:(1)“线桥法”表示电子转移情况,可以用“双线桥”也可以用“单线桥”。注意单线桥是直接由还原剂指向氧化剂,标明电子转移数目,不要标得失;
(2)氧化剂是得电子的物质,化合价降低,由方程式知道,Mn元素的化合价降低,则KMnO4是氧化剂,HCl是还原剂。
(3)该反应中16个HCl参与反应,转移10个e-,生成5个Cl2。则转移6.02×1023个电子,即1mol电子时,生成Cl2为0.5mol。
点评:双线桥要会熟练书写,注意检查得失电子总数相等的规律
