下列图示与对应的叙述相符的是
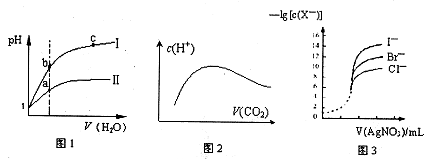
A.图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B.向溶质为1mol的NaOH溶液中通入CO2,随着CO2气体的通入,溶液中水电离出的c(H+)有如上图2变化关系
C.如上图2所示,水电离出c(H+)达到最大值时,溶液中各离子浓度大小分别为
c(Na+)>c(OH-)>c(CO32-)>c(HCO3-)>c(H+)
D.用0.0l00mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
答案:B
题目分析:A项中,图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释,pH的变化快的曲线是强酸,故曲线I为盐酸,说法错误;B项中,因为酸碱抑制水电离,盐的水解促进水电离,起始的NaOH溶液,水电离的c(H+)小,与CO2反应生成Na2CO3时水解,水电离的c(H+)最大,最后成为饱和的碳酸溶液,水电离出的c(H+)又减小,故图2正确;C项中,图2所示,水电离出c(H+)达到最大值是生成Na2CO3时,溶液中各离子浓度大小分应为c(Na+)>c(CO32-)>c(OH-) >c(HCO3-)>c(H+),故不正确;D项在,用0.0l00mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图3曲线可知c(I-)最小,可确定首先沉淀的是I-,说法错误。
