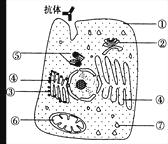
问题
选择题
已知在常温下测得浓度均为0.1 mol·L-1的下 * * 种溶液的pH:
| 溶质 | NaHCO3 | Na2CO3 | NaCN |
| pH | 9.7 | 11.6 | 11.1 |
下列说法中正确的是( )
A.阳离子的物质的量浓度之和:
Na2CO3>NaCN>NaHCO3
B.相同条件下的酸性:H2CO3<HCN
C.三种溶液中均存在电离平衡和水解平衡
D.升高Na2CO3溶液的温度,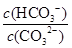 减小
减小
答案
答案:C
阳离子均为Na+和H+,Na2CO3溶液中Na+浓度是其他两种溶液的两倍,阳离子浓度最大,NaCN溶液和NaHCO3溶液中Na+浓度相等,NaCN溶液中H+浓度小于NaHCO3溶液,故阳离子浓度大小顺序为Na2CO3>NaHCO3>NaCN,A项错误;HCO3-的水解能力小于CN-,故酸性:H2CO3>HCN,B项错误;升高Na2CO3溶液的温度,促进其水解, 增大,D项错误。
增大,D项错误。