问题
选择题
下列各项说法中,不正确的是 ( )
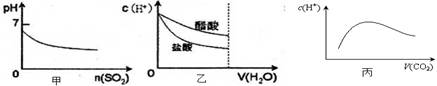
A.甲是向溴水通入SO2气体时,pH与SO2物质的量的关系图
B.乙是向c(H+)相同的醋酸和盐酸滴入水时,c(H+)与水体积的关系图
C.常温常压下,将2b mol CO2气体通入1L bmol·L-1的NaOH溶液中,随着CO2气体的通入,溶液中由水电离出的c(H+)有如丙图变化关系
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)>c(NO3-)
答案
答案:D
题目分析:A、溴水与二氧化硫反应生成溴化氢和硫酸,pH降低,A正确;B、盐酸是强酸,醋酸是弱酸,存在电离平衡,稀释促进电离,所以稀释相同的倍数时盐酸的pH变化大,B正确;C、二氧化碳与氢氧化钠反应生成碳酸钠,二氧化碳过量又生成碳酸氢钠。根据数量关系可知,最终得到的是碳酸氢钠和碳酸的混合液。氢氧化钠是强碱,抑制水的电离,而碳酸钠、碳酸氢钠均水解促进水的电离,但碳酸氢钠的水解程度小于碳酸钠的水解程度,因此图像不符合,C不正确;D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中根据电荷守恒可知c(Na+)+ c(H+)=c(OH-)+ c(Cl-)+>c(NO3-),c(H+)=c(Cl-),所以溶液中:c(Na+)>c(NO3-),D正确,答案选D。
