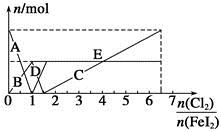
向FeI2溶液中不断通入Cl2,溶液中I-、I2、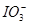 、Fe2+、Fe3+等粒子的物质的量随n(Cl2)∶n(FeI2)变化的曲线如图所示。
、Fe2+、Fe3+等粒子的物质的量随n(Cl2)∶n(FeI2)变化的曲线如图所示。
已知:2Fe3++2I-=I2+2Fe2+。
请回答下列问题:
(1)指出图中折线E和线段C所表示的意义:折线E表示 ;线段C表示 。
(2)写出线段D所表示的反应的离子方程式: 。
(3)当n(Cl2)∶n(FeI2)=6.5时,溶液中n(Cl-)∶n(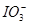 )= 。
)= 。
(1)n(Fe3+)随n(Cl2)∶n(FeI2)变化的情况
n(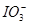 )随n(Cl2)∶n(FeI2)变化的情况
)随n(Cl2)∶n(FeI2)变化的情况
(2)Cl2+2Fe2+=2Fe3++2Cl-
(3)6.5
(1)有关物质的还原性顺序为I->Fe2+>I2,则向FeI2溶液中不断通入Cl2的过程中,依次发生的氧化还原反应为Cl2+2I-=2Cl-+I2,Cl2+2Fe2+=2Fe3++2Cl-,5Cl2+I2+6H2O=2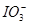 +12H++10Cl-。可见,当n(Cl2)∶n(FeI2)=1时,I-恰好全部被氧化;当n(Cl2)∶n(FeI2)=1.5时,Fe2+恰好全部被氧化;当n(Cl2)∶n(FeI2)=6.5时,氧化还原反应发生完毕。因此,当n(Cl2)∶n(FeI2)>1时,开始生成Fe3+,至n(Cl2)∶n(FeI2)=1.5时,n(Fe3+)达到最大值,故折线E代表了n(Fe3+)随n(Cl2)∶n(FeI2)变化的情况;当n(Cl2)∶n(FeI2)>1.5时,开始生成
+12H++10Cl-。可见,当n(Cl2)∶n(FeI2)=1时,I-恰好全部被氧化;当n(Cl2)∶n(FeI2)=1.5时,Fe2+恰好全部被氧化;当n(Cl2)∶n(FeI2)=6.5时,氧化还原反应发生完毕。因此,当n(Cl2)∶n(FeI2)>1时,开始生成Fe3+,至n(Cl2)∶n(FeI2)=1.5时,n(Fe3+)达到最大值,故折线E代表了n(Fe3+)随n(Cl2)∶n(FeI2)变化的情况;当n(Cl2)∶n(FeI2)>1.5时,开始生成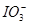 ,至n(Cl2)∶n(FeI2)=6.5时,n(
,至n(Cl2)∶n(FeI2)=6.5时,n(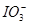 )达到最大值,故线段C代表了n(
)达到最大值,故线段C代表了n(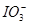 )随n(Cl2)∶n(FeI2)变化的情况。
)随n(Cl2)∶n(FeI2)变化的情况。
(2)当n(Cl2)∶n(FeI2)>1∶1时,Fe2+开始被氧化,当n(Cl2)∶n(FeI2)=1.5时,Fe2+恰好全部被氧化,故线段D代表了n(Fe2+)随n(Cl2)∶n(FeI2)变化的情况。线段D所发生反应的离子方程式为Cl2+2Fe2+=2Fe3++2Cl-。
(3)当n(Cl2)∶n(FeI2)=6.5时,根据元素守恒,可知溶液中n(Cl-)∶n(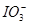 )=6.5。
)=6.5。
