问题
问答题 案例分析题
背景材料:
将pH=8和pH=10的两种氢氧化钠溶液等体积混合,混合后溶液中的c(H+)最接近于()mol/L。
A.(10-8+10-10)/2
B.(10-8+10-10)
C.(10-14-5×10-5)
D.2×10-10
问题:
(1)分析学生可能出现的解题错误及原因。
(2)本题正确答案为____,解题思路为____。
答案
参考答案:
(1)错误解答A。因为pH=8和pH=10的两种氢氧化钠溶液的c(H+)分别为10-8mol/L、10mol/L,而且两种溶液等体积混合,因此混合后溶液的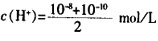 。
。
错解原因:直接应用溶液中c(H+)来求解,忽略溶液中c(OH-)>c(H+)和c(OH-)对水电离平衡的影响。
(2)正确答案D。解题过程:由于碱溶液中的c(OH-)>c(H+),这就决定了不能用混合前溶液中的c(H+)直接求混合后溶液的c(H+),一定要先求出混合后溶液中c(OH-),再换算成混合后的c(H+)。根据水离子积常数知,pH=8和pH=10的两种氢氧化钠溶液的c(OH-)分别为10-6mol/L和10-4mol/L,因此混合后溶液的c(OH-)=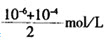 ,可近似看作为
,可近似看作为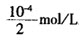 。根据水的离子积常数可知,混合后溶液的c(H+)=2×10-10mol/L,故正确答案选D。
。根据水的离子积常数可知,混合后溶液的c(H+)=2×10-10mol/L,故正确答案选D。
