问题
问答题 案例分析题
背景材料:
在反应中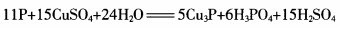 ,每摩尔CuSO4能氧化P的物质的量为()。
,每摩尔CuSO4能氧化P的物质的量为()。
A.1/5mol
B.2/5mol
C.3/5mol
D.11/5mol
上面是某教师设计的化学测试中的一道题。
问题:
(1)分析学生可能出现的解题错误及原因。
(2)本题正确答案为(),分析其正确的解题思路。
答案
参考答案:
(1)学生可能错选B。从化学方程式可以看出,15molCuSO4生成6molH3PO4,所以1molCuSO4生成2/5molH3PO4。错解原因:没有注意到生成物中的H3PO4有一半是P自身氧化还原反应(歧化反应)生成的。
(2)本题的正确答案是A。解题思路:题中的还原剂是P,而氧化剂是P和CuSO4。由于反应过程中Cu从+2降为+1,因此反应中共得到15mol的电子:而做还原剂的P在反应中从0升至+5价,因此1molP得到5mol电子。因此15molCuSO4在反应中氧化3mol的P,即每摩尔硫酸铜能够氧化0.2mol的P。
