阅读理解。
As is known, healthy foods can help save your life. Now, here is a list of healthy foods that can save your
memory. It is best that every person knows what he eats, as he takes in, can make or break himself, in terms
of health.
Fish is helpful in regaining back the kind of memory that a person once has. Eating fish can help you save
the trouble of forgetfulness. Vegetables rich in fiber and other dark and green leafy kinds are very suitable for
people who want to avoid mental blocks. These foods contain high units of vitamin E.
Another food that is considered having different effects on preventing this brain deficiency (缺陷) is
avocado (鳄梨), which is also rich in vitamins E and C. It is really good to know these healthy foods that can
save your memory are always at hand so as to help you in your fight against diseases. Sunflower seeds are
regarded as Vitamin C-powered seeds and also give you enough energy.
As for red wine, do not over consume it, as it is said to have to be taken in moderate amounts in order to
help the body. Over-drinking can cause illness and like anything else. This is considered as one of the healthy
foods that can save your memory; alcohol can otherwise lose it.
It is better to consume colored bread, rice and whole grains for you to get the best out of fiber. These
foods can lower the body's risk of being infected with Alzheimer's disease (老年痴呆病).
Knowing the healthy foods that can save your memory is living the life that you have longed and desired.
Among the others, the best, of course, is exercise. Taking in different kind of exercises, physical activities
or sports can keep both your body and mind healthy.
1. If you suffer from loss of memory, you _____.
A. should eat cucumbers and cabbages
B. can drink as much wine as possible
C. had better take in fish in your meals
D. may as well take more vitamin C
2. To prevent mental disease from happening, _____.
A. people are advised to take avocados
B. it is best to eat vegetables high in fiber
C. it is better to have more sunflower seeds
D. red wine is the first and best choice
3. Which of the following is the most important for health?
A. Drinking a proper amount of red wine every day.
B. Eating bread made of whole grains.
C. Adding Vitamin C-powered seeds to meals.
D. Taking moderate exercise every day.
4. How many means for health does the author mention in the passage?
A. Six.
B. Seven.
C. Eight.
D. Nine.
5. Which of the following is most suitable for the passage? (① = Para.l ②= Para.2③ = Para.3④ = Para.4
⑤= Para. 5⑥ = Para. 6)
A. 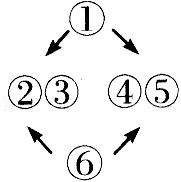 B.
B. 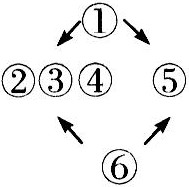 C.
C. 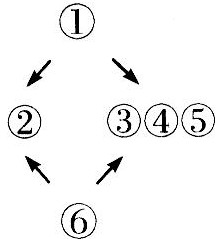 D.
D. 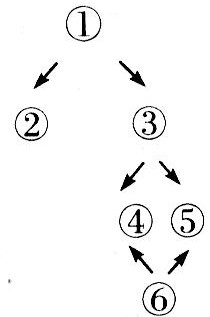
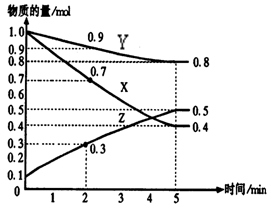
 2Z (2)0.05mol·L-1·min-1
2Z (2)0.05mol·L-1·min-1 2Z;
2Z; 2Z可 * * 段式如下:
2Z可 * * 段式如下: 2Z
2Z
 B.
B.  C.
C.  D.
D. 