(14分 每空2分)化工原料红矾钠(重铬酸钠:Na2Cr2O7·2H2O)主要是以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3、SiO2等杂质)为主要原料生产,其主要工艺流程如下:
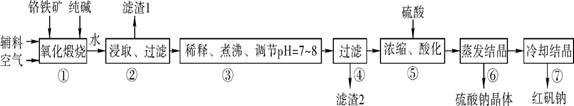
步骤①中主要反应的化学方程式如下:
4FeO·Cr2O3+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
(1) ①中反应是在回转窑中进行的,反应时需不断搅拌,其作用是 。
(2) 杂质Al2O3在①中转化的化学反应方程式为 。
(3) 用化学平衡移动原理说明③中煮沸的作用是 (用离子方程式结合文字说明),若调节pH过低产生的影响是 。
(4) ⑤中酸化是使CrO42-转化为Cr2O72-写出该反应的离子方程式: 。

(5) 工业上还可用电解法制备重铬酸钠,其装置示意图如上。
阴极的电极反应式为 ;
阳极的电极反应式为 。
(14分 每空2分) (1) 增大反应物的接触面积,加快反应速率
(2) Al2O3+Na2CO3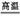 2NaAlO2+CO2↑
2NaAlO2+CO2↑
(3) 水解吸热,煮沸促进水解平衡AlO2-+2H2O Al(OH)3+OH-、SiO32-+2H2O
Al(OH)3+OH-、SiO32-+2H2O H2SiO3+2OH-向右移动,生成氢氧化铝、硅酸沉淀
H2SiO3+2OH-向右移动,生成氢氧化铝、硅酸沉淀
H+将水解生成的氢氧化铝沉淀溶解,杂质Al3+与Na2CrO4难以分离
(4) 2CrO42-+2H+ Cr2O72-+H2O
Cr2O72-+H2O
(5) 4H2O+4e- 4OH-+2H2↑(H+放电也可)
4OH-+2H2↑(H+放电也可)
4OH--4e- O2↑+2H2O
O2↑+2H2O
题目分析:(1) 固体反应物在搅拌时,可以与氧气充分接触,增大接触面积,使反应速率加快;
(2)氧化铝与碳酸钠在高温条件下发生反应,生成偏铝酸钠和二氧化碳,化学方程式为Al2O3+Na2CO3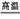 2NaAlO2+CO2↑
2NaAlO2+CO2↑
(3)氧化煅烧再溶于水,所得溶液中有偏铝酸钠、硅酸钠、铬酸钠,其中AlO2-、SiO32-水解,水解吸热,煮沸促进水解平衡AlO2-+2H2O Al(OH)3+OH-、SiO32-+2H2O
Al(OH)3+OH-、SiO32-+2H2O H2SiO3+2OH-向右移动,生成氢氧化铝、硅酸沉淀;若溶液pH过低,则生成的氢氧化铝沉淀又溶解生成Al3+,杂质Al3+与Na2CrO4难以分离;
H2SiO3+2OH-向右移动,生成氢氧化铝、硅酸沉淀;若溶液pH过低,则生成的氢氧化铝沉淀又溶解生成Al3+,杂质Al3+与Na2CrO4难以分离;
(4)酸性条件下CrO42-转化为Cr2O72-,该反应是可逆反应,离子方程式为2CrO42-+2H+ Cr2O72-+H2O;
Cr2O72-+H2O;
(5)电解池中阴极是阳离子放电,根据离子的放电顺序,应是氢离子放电,所以电极反应式为4H2O+4e- 4OH-+2H2↑;或2H++2e-= H2↑;阳极是阴离子放电,所以是氢氧根离子放电,电极反应式为4OH--4e-
4OH-+2H2↑;或2H++2e-= H2↑;阳极是阴离子放电,所以是氢氧根离子放电,电极反应式为4OH--4e- O2↑+2H2O。
O2↑+2H2O。
