(17分)某反应A(g)+B(g) C(g)在任一时刻的正、逆反应速率可用υ正、υ逆表示:
C(g)在任一时刻的正、逆反应速率可用υ正、υ逆表示:
υ正=k1·c(A)·c(B),υ逆=k2·c(C),其中k1、k2在一定温度下为常数,c(A)、c(B)、c(C)分别代表某时刻三种物质的物质的量浓度。
(1)上述反应达到平衡时,请用题干中的符号分别表示三种物质的浓度关系为 ,
平衡常数K=_ __。
(2)在300 K时,开始反应的A、B浓度均为0.1 mol/L,达到平衡时B的转化率为50%,则k1、k2之间的关系是__________________。
(3)升高温度,k1的变化是 ,k2的变化是_________(填“增大”、“减小”或“不变”);此时若k1/k2增大,则说明正反应是___________(填“吸”或“放”)热反应。
(4) CO2可与H2合成绿色燃料甲醇。300oC时,在两个容积均为2L的密闭容器中,当c(CO2)=1.00 mol·L-1、c(H2)=1.60 mol·L-1时,分别选择催化剂Ⅰ、催化剂Ⅱ开始反应,t0时达到平衡状态M1、M2。若υ逆(M1)<υ正(M2)。且达M1时,CO2的转化率为20%,请画出两个状态的浓度商(Qc)-时间(t)的关系图像,并标明相关数据。
=
(5)实验室可利用甲醇、空气、铜(或氧化铜)制备甲醛。关于甲醇和甲醛的沸点和水溶性见下表:
| 沸点 | 水溶性 | |
| 甲醇 | 65℃ | 与水相溶 |
| 甲醛 | -21℃ | 与水相溶 |
a.热水浴加热 b.冰水浴冷却 c.酒精灯加热 d.酒精喷灯灼烧 e.常温即可
实验临近结束时,挤压D处气球使空气进入装置,该操作的目的是____________________。
(17分)
⑴k1·c(A)·c(B) =k2·c(C)(2’)。k1/k2(2’)。
⑵k1=20k2(2’)
⑶增大(1’),增大(1’);吸(1’)
⑷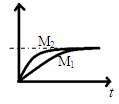 (2’
(2’
0.05 0 |
t |
题目分析:(1)反应达到平衡时,正反应速率等于逆反应速率,所以k1·c(A)·c(B) =k2·c(C);该式进行变形可得平衡常数K="c(C)/" c(A)·c(B)= k1/k2
(2)根据“三段式”进行计算:A(g) + B(g)  C(g)
C(g)
初始浓度(mol•L‾1) 0.1 0.1 0
转化浓度(mol•L‾1) 0.05 0.05 0.05
平衡浓度(mol•L‾1) 0.05 0.05 0.05
根据平衡时k1·c(A)·c(B) =k2·c(C),可得0.05×0.05 k1=0.05×k2,解得k1=20k2
(3)升高温度,化学反应速率都加快,所以k1与k2都增大;若k1/k2增大,说明正反应速率增加的倍数大,则正反应速率大于逆反应速率,即升高温度,平衡向正反应方向移动,所以正反应是吸热反应。
(4)催化剂只改变反应速率,不影响化学平衡,所以达到平衡时M1、M2相同,即平衡时两条曲线重合,因为υ逆(M1)<υ正(M2),所以催化剂Ⅱ催化效果更好,反应速率更快,可画出图像。
