问题
问答题
有一种烃类物质,为了测定其组成,做了以下测试:
①同温同压条件下,测得它的密度是H2密度的43倍;
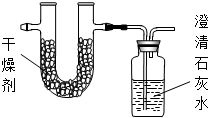
②将1.72克该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
| 实验前 | 实验后 | |
| (干燥剂+U型管)的质量 | 101.1g | 103.62g |
| (石灰水+广口瓶)的质量 | 312.0g | 317.28g |
(2)写出该烃所有可能的结构简式.
答案
(1)由n=
=m M
可知相对密度之比等于相对分子质量之比,确定该烃的相对分子质量为2×43=86,V Vm
所以1.72克该烃的物质的量为
=0.02mol,1.72g 86g/mol
由表中数据可知,干燥管增重的质量为水的质量,则n(H2O)=
=0.14mol,n(H)=0.28mol,103.62g-101.1g 18g/mol
广口瓶增重的质量为二氧化碳的质量,则n(CO2)=
=0.12mol,317.28g-312.0g 44g/mol
则1mol烃中含有
=14molH原子,含有0.28mol 0.02
=6molC原子,0.12mol 0.02
所以分子式为C6H14,
答:确定该烃的相对分子质量为86和化学式为C6H14.
(2)该烃为己烷,可能的结构简式有:
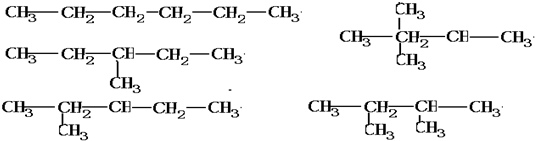
,
答:可能的结构简式有:
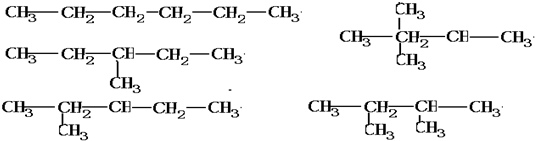
.
