(1)下列说法正确的是______
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然发生能量的变化
B.钢铁的吸氧腐蚀和析氢腐蚀的负极反应都为Fe-2e-=Fe2+
C.放热反应发生时不一定要加热,但吸热反应必须要加热才能发生
D.可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物不再转化为生成物
(2)25℃、101kPa条件下,8gCH4气体完全燃烧生成CO2气体和液态水放出445kJ热量.
写出CH4燃烧的热化学方程式______
(3)101kPa条件下,氮气和氢气反应生成氨气的能量变化如图示意:
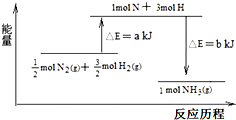
又已知:①a=1127;②25℃、101kPa下N2(g)+3H2(g)=2NH3(g)△H=-92kJ•mol-1则b=______.
(1)A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,由于反应物和生成物的能量不等,必然发生能量的变化,故A正确;
B.钢铁的吸氧腐蚀和析氢腐蚀的负极反应都是金属失去电子,电极反应为:Fe-2e-=Fe2+,故B正确;
C.放热反应发生时不一定要加热,但吸热反应也不一定要加热,故C错误;
D.可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物仍然转化为生成物,故D错误;
故选:AB;
(2)8gCH4气体完全燃烧生成CO2气体和液态水放出445kJ热量,16g即1molCH4在氧气中燃烧生成CO2和液态水,放出889kJ热量,则热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890KJ/mol,
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890KJ/mol;
(3)该反应放热,反应热=反应物的键能-生成物的键能,氮气和氢气反应生成氨气的热化学方程式为:
N2(g)+1 2
H2(g)=NH3(g)△H=a-bkJ•mol-1,则N2(g)+3H2(g)=2NH3(g)△H=2(a-b)kJ•mol-1=-92kJ•mol-1,所以a-b=-46,又因a=1127,所以a-b=-46,b=1173,故答案为:1173;3 2

