问题
多选题
某化合物64g在氧气中完全燃烧,只生成88gCO2和72gH2O.下列说法正确的是( )
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1:4
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
答案
88gCO2的物质的量=
=2mol,88g 44g/mol
72gH2O的物质的量=
=4mol,72g 18g/mol
根据原子守恒可知该化合物中C、H原子数目之比=2mol:4mol×2=1:4,
该混合物质C元素质量=2mol×12g/mol=24g、H元素的质量=4mol×2×1g/mol=8g,C、H元素的质量之和为24g+8g=32g<60g,故该化合物中还含有氧元素,
故选BD.

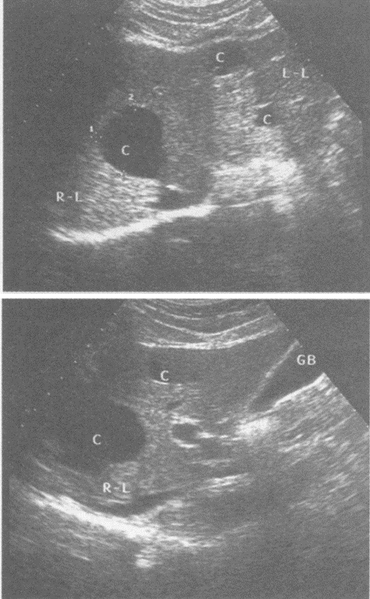 超声提示()。
超声提示()。