根据下列材料,按要求完成任务。
材料一《义务教育化学课程标准(2011年版)》的内容标准:认识燃烧、缓慢氧化和爆炸发生的条件,了解防火灭火、防范爆炸的措施。
材料二教科书的知识结构体系
绪言化学使世界变得更加绚丽多彩
第一单元走进化学世界
第二单元我们周围的空气
第三单元物质构成的奥秘
第四单元自然界的水
第五单元化学方程式
第六单元碳和碳的氧化物
第七单元燃料及其利用
课题1燃烧和灭火
课题2燃烧和热量
课题3使用燃料对环境的影响
拓展性课题石油和煤的综合利用
第八单元金属和金属材料
第九单元溶液
第十单元酸和碱
第十一单元盐化肥
第十二单元化学与生活
材料三教科书关于“燃烧和灭火”的部分内容
一、燃烧的条件
【实验7-1】在500mL的烧杯中注入400mL热水,并放入用硬纸圈圈住的一小块白磷。在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷(如图7-4),观察现象。

用导管对准上述烧杯中的白磷,通入少量氧气(或空气),观察现象。

讨论
1.由上述实验中薄铜片上的白磷燃烧而红磷不燃烧的事实,说明燃烧需要什么条件?
2.由薄铜片上的白磷燃烧而热水中的白磷不燃烧的事实,说明燃烧还需要什么条件?
3.由本来在热水中不燃烧的白磷,在通入氧气(或空气)后燃烧的事实,再次说明燃烧需要什么条件?
4.综合上述讨论,可得出燃烧需要哪些条件?
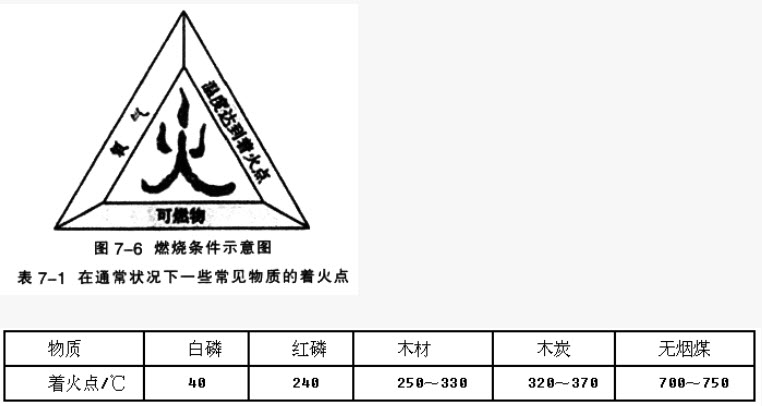
可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫作燃烧,燃烧需要三个条件:
(1)可燃物;
(2)氧气(空气);
(3)达到燃烧所需要的最低温度(也叫着火点)。
二、灭火的原理和方法
如果破坏燃烧的条件,使燃烧反应停止,就可以达到灭火的目的。

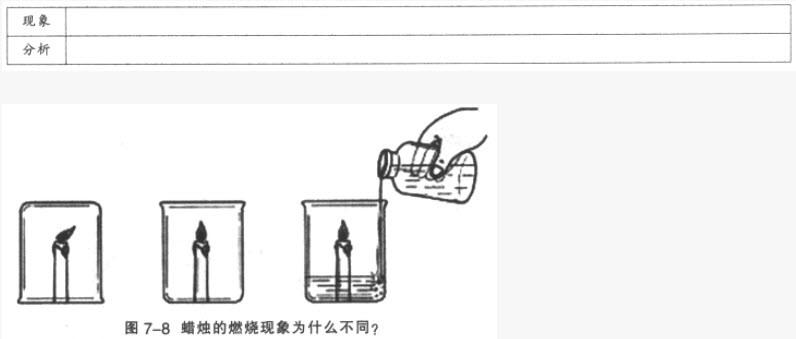
【实验7-2】点燃三支蜡烛,在其中一支蜡烛上扣一只烧杯;将另两支蜡烛放在烧杯,然后向其中一只烧杯中加适量碳酸钠和盐酸(如图7-8),观察现象并分析原因。
清除可燃物或使可燃物与其他物品隔离,隔绝氧气(或空气),以及使温度降到着火点以下,都能达到灭火的目的。
要求:
(1)试确定本节课的三维教学目标。
(2)试确定本节课的教学重点和难点。
(3)同一个化学实验课题,可以设计出多种实验方案,这就需要进行选择。请简述如何根据化学实验设计的原则和中学化学教学的实际优选实验方案?
(4)依据材料,设计本节课的教学过程。
(5)请对本节课的内容进行板书设计。
参考答案:
(1)三维教学目标:
①知识与技能目标:初步认识燃烧现象,知道物质燃烧的必须条件;了解灭火的原理,学会常见的灭火方法。
②过程与方法目标:能利用燃烧的条件解释日常生活中的现象;能利用灭火的原理,处理一些突发的失火状况:进一步学习科学探究的一般方法与步骤,学会科学探究的思考方法。
③情感态度与价值观:通过探究“燃烧的条件”,初步形成富于思考、勇于探索的科学精神;通过学习辨证地认识燃烧现象,体会到学习化学的价值。
(2)教学重点:燃烧条件和灭火原理。
教学难点:燃烧条件的实验探究。
(3)根据化学实验设计的原则和中学化学教学的实际,可确定如下优选标准:效果明显;绿色化,操作安全;装置简单:易操作、用药少;步骤少、时间短。
(4)教学过程
[故事导入]
1854年5月30日,英国战舰“欧罗巴”号,按照作战命令开始了远涉重洋的航行,它的船舱里结结实实地装满了供战马吃的草料。两个多月后,船舱突然冒出熊熊大火,大火迅速吞没了整艘战舰,片刻之间战舰便葬身海底,全舰官兵、战马无一生还……事后化学家们根据英国军事保安部门提供的材料,准确地找到了“纵火犯”——草料。草料是怎么成为纵火犯的呢?通过这节课的学习,我们就能解决这个问题。
[新课讲授,探究新知]
环节1:复习燃烧的概念。
学生回顾以前学的旧知识(物质在氧气中的燃烧)得出燃烧是一种发光、发热、剧烈的化学反应的概念。
环节2:探究燃烧的条件,感知实验事实,并分析归纳燃烧的条件。
这里通过水与酒精的燃烧对比实验,引导学生思考并讨论,得出燃烧需要可燃物的结论。
对比实验【7-1】,铜片上的白磷燃烧,红磷不燃烧,水下白磷不燃烧。引导学生思考并讨论,得出燃烧需要与空气或氧气接触,并达到可燃物的着火点。
学生思考并讨论让水下白磷燃烧的方法,教师听取意见后,演示热水下的白磷在通入氧气后燃烧的实验。
[联系整合,巩固新知]
教师展示象征燃烧条件的“火三角”教具,通过对教具的拼合演示,让学生对前面所学知识进一步升华与沉淀,认识到燃烧的三个条件缺一不可。
通过我们这节课的学习,思考前面故事中的草料为什么会燃烧起来?
小组讨论、合作交流后解释原因,教师评价。
[投影]展示化学家的解释:
草料会和空气中的氧发生氧化反应,这种氧化反应进行得很缓慢,不像燃烧那样剧烈地发光发热,叫缓慢氧化。物质在缓慢氧化的过程里也产生热,不过放热速度很慢,平时觉察不出来。由于“欧巴罗”号船舱里堆放的草料太多太实,空气不流通,缓慢氧化产生的热量不易散发,越积越多,温度逐渐升高,达到了草料的着火点。可燃物在具备跟氧气接触、温度达到着火点的条件下,不经点燃便自行燃烧起来。
本节课中大家看到的白磷,它的着火点只有40℃,所以在实验室中,我们通常把白磷保存在水中以隔绝空气。
[小结作业]
总结本节课内容,联系点燃火柴的过程,思考以下几个问题:
划火柴是为了达到什么目的?除了摩擦,还有什么过程可以达到使火柴头燃烧的目的?火柴头是什么制作的?如果换成煤作火柴头可不可以?
(5)板书设计:

