问题
填空题
一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g) H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
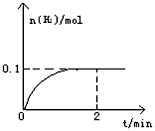
(1)0-2min内的平均反应速率v(HI)=_________。该温度下,H2(g)+I2(g) 2HI(g)的平衡常数K=_________。
2HI(g)的平衡常数K=_________。
(2)相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则_________是原来的2倍。
a.平衡常数 b.HI的平衡浓度 c.达到平衡的时间 d.平衡时H2的体积分数
(3)以H2为燃料可制成氢氧燃料电池。 已知2H2(g)+O2(g)==2H2O(l) △H=-572kJ/mol-1
某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为___________。
答案
(1)0.1mol·L·min;80
(2)bd
(3)80%
