(10分)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
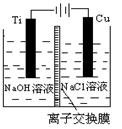
| 方法Ⅱ | 电解法,反应为2Cu + H2O 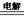 Cu2O + H2↑。 Cu2O + H2↑。 |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H = -169kJ·mol-1
C(s)+1/2O2(g)="CO(g) " △H = -110.5kJ·mol-1
Cu(s)+1/2O2(g)="CuO(s) " △H = -157kJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H = ▲ kJ·mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为 ▲ 。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放 出N2。该制法的化学方程式为 ▲ 。
出N2。该制法的化学方程式为 ▲ 。
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验: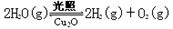 △H>0,水蒸气的浓度随时间t变化如下表所示。
△H>0,水蒸气的浓度随时间t变化如下表所示。
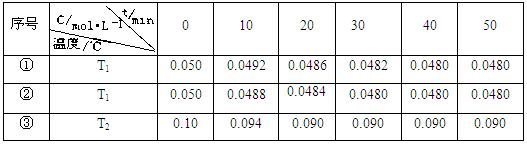
下列叙述正确的是 ▲ (填字母代号)。
A.实验的温度:T2<T1
B.实验①前20 min的平均反应速率v(H2)=7×10-5 mol·L-1 min—1
C.实验②比实验①所用的催化剂催化效率高
(每空2分,共10分)(1)反应不易控制,易还原产生Cu
(2)+34.5 (3)2Cu-2e-+2OH-=Cu2O+H2O
(4)4Cu(OH)2 + N2H4 2Cu2O + N2↑ + 6H2O (5)BC
2Cu2O + N2↑ + 6H2O (5)BC
