氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用。
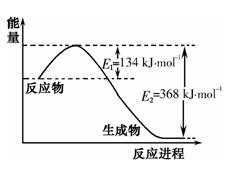
(1)下图是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2气体和CO反应的热化学方程式: 。
(2)已知: CO(g)+1/2 O2(g) = CO2(g) △H = -283 kJ/mol
N2(g)+ O2(g) =" " 2 NO(g) △H = +180 kJ/mol
则反应2 NO(g)+2 CO(g) N2(g) + 2 CO2(g) △H = kJ/mol。
N2(g) + 2 CO2(g) △H = kJ/mol。
(3)在固定体积的密闭容器中,进行如下化学反应: N2(g)+3H2(g) 2NH3(g);△H<0,其平衡常数K与温度T的关系如下表:
2NH3(g);△H<0,其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
② 试判断K1 K2(填写“>”“=”或“<”)
③下列各项能说明该反应一定达到平衡状态的是 (填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(H2)(逆) =)3v(N2)(正)
c.容器内压强保持不变 d.混合气体的密度保持不变
④若上述反应达到平衡时,N2、H2、NH3的浓度之比为1:3:2,再向容器中按物质的量之比为1:3:2通入N2、H2、NH3,与原平衡相比,N2的物质的量浓度 (填增大、不变或减小,下同),NH3的体积分数 。
(1)NO2(g)+CO(g) ==CO2(g)+NO(g) △H=-234kJ·mol-1(2分)
(2)-746(2分)
(3)①K=c2(NH3)/[c(N2)×c3(H2)](1分) ② >( 1分) ③ bc(2分)
(4)增大 增大 (各1分)
