问题
选择题
含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=" +28.7" kJ·mol-1
B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H= _28.7 kJ·mol-1
C.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H="+57.4" kJ·mol-1
D.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H= _57.4 kJ·mol-1
答案
答案:D
20.0gNaOH是0.5mol,与足量稀盐酸反应,放出28.7 kJ的热量,则1molNaOH反应,放热28.7*2=57.4kJ。根据热化学方程式的书写原则进行判断。
A项,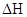 的符号和数值均不正确。
的符号和数值均不正确。
B项,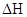 的数值不正确。
的数值不正确。
C项,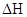 的符号不正确。
的符号不正确。
D项,符合热化学方程式的书写原则,正确。
故选D
