阅读下面的文言文,完成下面的题。
盖延字巨卿,渔阳要阳人也。身长八尺,弯弓三百斤。边俗尚勇力,而延以气闻。
及王郎起,延与吴汉同谋归光武。光武即位,以延为虎牙 * * 。
建武二年,更封安平侯。遣南击敖仓,转攻酸枣、封丘,皆拔。其夏,督马武、刘隆、马成、王霸等南伐刘永,围永于睢阳。数月,尽收野麦,夜梯其城入。永惊惧,引兵走出东门,延追击,大破之。永弃军走谯,延进攻,拔薛,斩其鲁郡太守,又破永沛郡太守,斩之。永将苏茂、佼强、周建等三万余人救永,共攻延,延与战于沛西,大破之。永军乱,遁没溺死者大半。永弃城走湖陵,苏茂奔广乐。
三年,睢阳复反城迎刘永,延复率诸将围之百日,收其野谷。永乏食,突走,延追击,尽得辎重。永为其将所杀,永弟防举城降。
四年春,延又击苏茂、周建于蕲,进与董宪战留下,皆破之。因率平狄 * * 庞萌攻西防,拔之。复追败周建、苏茂于彭城,茂、建亡奔董宪,董宪将贲休举兰陵城降。宪闻之,自郯围休。时,延及庞萌在楚,请往救之。帝敕曰:“可直往捣郯,则兰陵必自解。”延等以贲休城危,遂先赴之。宪逆战而阳败,延等逐退,因拔围入城。明日,宪大出兵合围,延等惧,遽出突走,因往攻郯。帝让之曰:“间欲先赴郯者,以其不意故耳。今既奔走,贼计已立,围岂可解乎!”延等至郯,果不能克,而董宪遂拔兰陵,杀贲休。帝以延轻敌深入,数以书诫之。及庞萌反,攻杀楚郡太守,引军袭败延,延走,北渡泗水,破舟楫,坏津梁,仅而得免。帝自将而东,征延与吴汉、王常、王梁、马武、王霸等会任城,讨庞萌于桃乡,又并从征董宪于昌虑,皆破平之。六年春,遣屯长安。
十一年,与中郎将来歙攻河池,未克,以病引还,拜为左冯翊, * * 如故。十三年,增封定食万户。十五年,薨于位。(节选自范晔《后汉书·吴盖陈臧列传》第八)
1.对下列句子中加粗词的解释,正确的一项是( )
A.边俗尚勇力/尚:尚且,更加
B.宪逆战而阳败/逆:掉头,反过来
C.帝让之曰/让:宽容,谦让
D.拜为左冯翊/拜:拜访,走访
2.以下句子分别编为四组,全部表现盖延勇武善战、勇往直前的一组是( )
①尽收野麦,夜梯其城入
②延进攻,拔薛,斩其鲁郡太守
③遽出突走,因往攻郯
④遁没溺死者大半
⑤延复率诸将围之百日
⑥北渡泗水,破舟楫,坏津梁
A.①②⑤
B.②③④
C.③④⑥
D.①⑤⑥
3.下列对原文内容的叙述和分析概括,不正确的一项是( )
A.盖延由于自身的条件、边地的风俗,而以气势闻名。随后,王郎起兵举事时归顺光武帝,当上了虎牙 * * 。
B.建武二年和三年,盖延攻城掠地,击败敌人、杀死郡守,取得了一个又一个胜利,显示出了他非凡的军事才能。
C.盖延曾在军事上受挫,在救援贲休这件事上,他由于没有听取光武帝的意见,结果中了董宪的计,兰陵未解围,郯城也未攻下。
D.盖延兰陵败退后,重整旗鼓,主动召集吴汉、王常、王梁、马武、王霸等共同讨伐庞萌、董宪,最后打败平定了他们。
4.把文中画线的句子翻译成现代汉语。
(1)永为其将所杀,永弟防举城降。
_____________________________________________________
(2)欲先赴郯者,以其不意故耳。
_____________________________________________________
(3)帝以延轻敌深入,数以书诫之。
_____________________________________________________
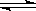 2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是