问题
计算题
恒温条件下,将2.0molSO2与amolO2混合通入一密闭容器中,发生如下反应:
2SO2(g)+O2(g) 2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。求:
2SO3(g)。反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol。求:
(1)a的值。
(2)平衡时SO2的转化率。
答案
(1)解:2SO2(g)+O2(g)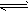 2SO3(g)
2SO3(g)
起始 2.0mol amol 0mol
变化 1.3mol 0.65mol 1.3mol
平衡 0.7mol 3.0mol 1.3mol
则a=3.0mol +0.65mol=3.65mol
(2)平衡时SO2的转化率=1.3/2.0×100%=65%
