问题
问答题
t℃时,将3molA和1molB气体通入容积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g)
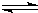
xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol•L-1.请计算:
(1)从反应开始到平衡状态,生成C的平均反应速率;
(2)x的值.
答案
(1)2min时反应达到平衡状态,容器C的浓度为0.4mol•L-1,
所以C的平均反应速率v(C)=
=△c △t
=0.2mol/(L•min),0.4mol/L 2min
答:C的平均反应速率为0.2mol/(L•min);
(2)参加反应的B的物质的量为1mol-0.8mol=0.2mol,
生成的C的物质的量为0.4mol•L-1×2L=0.8mol,
所以0.2mol:0.8mol=1:x,
解得x=4,
答:x的值为4.
