问题
选择题
已知
(1)H2( g )+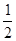 O2 ( g ) = H2O ( g ) ΔH1 =" a" kJ/mol
O2 ( g ) = H2O ( g ) ΔH1 =" a" kJ/mol
(2)2H2( g )+O2 ( g ) =2H2O ( g ) ΔH2 =" b" kJ/mol
(3) H2( g )+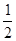 O2 ( g ) = H2O ( l ) ΔH3 =" c" kJ/mol
O2 ( g ) = H2O ( l ) ΔH3 =" c" kJ/mol
(4) 2H2( g )+O2 ( g ) =2H2O ( l ) ΔH4 =" d" kJ/mol
则a、b、c、d的关系正确的是( )。
A.c<a<0
B.b>d>0
C.2a=b< 0
D.2c=d>0
答案
AC
氢气燃烧是放热反应,△H小于0。由于参加反应的氢气越多,放热越多,所以2a=b<0,2c=d<0。又因为气态水的能量高于液态水的能量,所以氢气燃烧生产液态水放出的能量多,所以2c=d<2a=b<0,因此正确的答案选AC。
