问题
填空题
常温、常压下,可发生如下反应:A(g)+B(g)
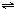
C(g)+nD(g),若将2molA和2molB混合充入体积可变的密闭容器中,在不同条件下达到平衡时,C的浓度如下:
| 温度/℃ | 压强/Pa | C平衡浓度/mol•L-1 |
| 25 | 1×105 | 1.0 |
| 25 | 2×105 | 1.8 |
| 25 | 4×105 | 3.2 |
| 25 | 5×105 | 6.0 |
(2)在5×105Pa时,D的状态为______.
答案
解析:(1)根据PV=nRT,温度、物质的量一定时,P1:P2=V2:V1.若P1:P2=1×105 Pa:2×105 Pa=1:2,则对应V2:V1=1:2,即体积变小一半,C的浓度应增大1倍,由1mol•L-1变为2mol•L-1.但是由于平衡移动变成1.8mol•L-1,压强增加到2倍,C的浓度只增加到1.8倍说明平衡向逆反应方向移动,逆反应是气体物质的量减少的反应,故n>1.
故答案为:n>1;压强增加到2倍,C的浓度只增加到1.8倍说明平衡向逆反应方向移动,逆反应是气体物质的量减少的反应,故2<n+1.
(2)将压强由1×105 Pa变为4×105 Pa时,仍符合以上规律.将压强由4×105 Pa变为5×105 Pa时,P1:P2=4:5,C的浓度应为3.2×
=4 mol•L-1.但平衡时,C的浓度增加到6mol•L-1,说明平衡向正反应方向移动.若D为气体,则不可能.只有在A、B、C为气体,D不为气体时,才符合题意,故D为固体或液体.5 4
故答案为:固体或液体
