(13分)使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到100mL ___________(填仪器名称)中定容,摇匀即得。
(2)用 取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴 作指示剂。
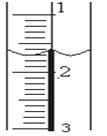
3)读取盛装0.1000 mol/L NaOH 溶液的 (填仪器名称)的初始读数。如果液面位置如右图所示,则此时的读数为 ml。
4)滴定。当 时,停止滴定,并记录NaOH溶液的最终读数。再重复滴定3次。
Ⅱ.实验记录
| 滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(5)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积 V =" [(15.95+15.00+15.05+14.95)" /4 ]mL = 15.24mL。
指出他的计算的不合理之处: 。
(6)乙同学仔细研究了该品牌白醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的 (填写序号)。a.pH b.沸点 c.电离常数 d.溶解度
(7)在本实验的滴定过程中,下列操作会使实验结果偏大的是 (填写序号)。
a.未用标准NaOH溶液润洗滴定管
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d. 锥形瓶在滴定时剧烈摇动,有少量液体溅出
(1)容量瓶 (2)酸式滴定管 酚酞 (3)碱式滴定管 1.70
(4)溶液由无色恰好变为红色,并在半分钟内不褪色
(5)第一组数据与后3组数据相差较大,属异常值,应舍去
(6)c (7)ab
题目分析:(1)配制一定物质的量浓度溶液的仪器是容量瓶。
(2)白醋显酸性,应该用酸式滴定管量取。醋酸和氢氧化钠反应后溶液显碱性,所以选择酚酞作指示剂。
(3)氢氧化钠溶液应该用碱式滴定管量取。由于滴定管的刻度自上而下逐渐增大,所以根据装置图可知,此时的读数是1.70ml。
(4)酸使酚酞试液显无色,碱使酚酞试液显红色,所以终点时的现象是溶液由无色恰好变为红色,并在半分钟内不褪色。
(5)根据表中数据可知,第一组数据与后3组数据相差较大,属异常值,应舍去。
(6)根据较强的酸制取减弱的酸可知,要判断醋酸和苯甲酸钠能否反应,只需要根据醋酸和苯甲酸的电离常数即可,答案选c。
(7)未用标准NaOH溶液润洗滴定管,则氢氧化钠溶液被稀释,消耗氢氧化钠溶液的体积增加,所以测定结果偏高;碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,说明消耗氢氧化钠溶液的体积增加,所以测定结果偏高;锥形瓶中加入待测白醋溶液后,再加入少量水,并没有改变醋酸的物质的量,不影响测定结果;锥形瓶在滴定时剧烈摇动,有少量液体溅出,则醋酸减少,消耗氢氧化钠溶液的体积减少,测定结果偏低,答案选ab。
点评:中和滴定误差分析的总依据为:由C测==C标V标/V测由于C标、V待均为定植,所以C测的大小取决于V标的大小,即V标:偏大或偏小,则C测偏大或偏小。根据产生误差的来源,从以下几个方面来分析:①洗涤误差。②读数误差。③气泡误差。④锥形瓶误差。⑤变色误差。⑥样品中含杂质引起的误差,这种情况要具体问题具体分析。
