某兴趣小组为探究外界条件对可逆反应 A(g)+B(g)
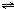
C(g)+D(s)的影响,在恒温条件下往一个容积为10L的密闭容器中充入1molA和1molB,反应达平衡时测得容器中各物质的浓度为I然后每次改变一种反应条件做了另三组实验,重新达到平衡时容器中各成分的浓度(其中D用物质的量来表达)分别为Ⅱ.Ⅲ.Ⅳ.
| A | B | C | D | |
| Ⅰ | 0.05mol•L-1 | a mol•L-1 | 0.05mol•L-1 | b mol |
| Ⅱ | 0.078mol•L-1 | 0.078mol•L-1 | 0.122mol•L-1 | m mol |
| Ⅲ | 0.06mol•L-1 | 0.06mol•L-1 | 0.04mol•L-1 | n mol |
| Ⅳ | 0.07mol•L-1 | 0.07mol•L-1 | 0.098mol•L-1 | p mol |
A.Ⅰ中a=1
B.实验Ⅳ结果的产生可能是因为采用从生成物配比的方法,且p≥0.98
C.Ⅱ对应的操作方法可以是在Ⅰ的基础上压缩反应容器的体积,且m>0.5
D.将Ⅲ与I比较,可以判断出正反应一定是放热反应
在恒温条件下往一个容积为10L的密闭容器中充入1molA和1molB,反应达平衡时,消耗的B的物质的量与A的物质的量相等,故a=0.05mol•L-1;
Ⅰ组:K=
=20L/mol,转化率=0.05mol•L-1 0.05mol•L-1×0.05mol•L-1
×100%=50%;0.05×10 1
Ⅱ组:K=
=20L/mol,但不能计算转化率,因体积不是10L,0.122mol•L-1 0.078mol•L-1×0.078mol•L-1
否则C的物质的量为0.122mol/L×10L>1mol,不符合题意,应为缩小体积,温度不变;
Ⅲ组:K=
=11.11L/mol,转化率=0.04mol•L-1 0.06mol•L-1×0.06mol•L-1
×100%=40%;0.04×10 1
Ⅳ组:K=
=20L/mol,但不能计算转化率,因体积不是10L,否则0.07mol/L×10L+0.098mol/L×10L>1mol,可能为缩小体积,或用从生成物配比的方法,温度不变.0.098mol•L-1 0.07mol•L-1×0.07mol•L-1
A、在恒温条件下往一个容积为10L的密闭容器中充入1molA和1molB,反应达平衡时,消耗的B的物质的量与A的物质的量相等,故a=0.05mol•L-1,故A错误;
B、实验Ⅳ中K=
=20L/mol,温度不变,因0.07mol/L×10L+0.098mol/L×10L>1mol,可能为缩小体积,或用从生成物配比的方法,如用从生成物配比的方法,反应如从逆向开始,因D为固体,对平衡无影响,如生成A、B为0.07mol/L×10L=0.7mol,D应>0.7mol,故B错误;0.098mol•L-1 0.07mol•L-1×0.07mol•L-1
C、Ⅱ组:K=
=20L/mol,但不能计算转化率,因体积不是10L,否则C的物质的量为0.122mol/L×10L>1mol,不符合题意,应为缩小体积,与Ⅰ组相比较,Ⅰ组达到平衡时D的物质的量为0.5mol,而Ⅱ组压强较大,增大压强平衡向正方向移动,平衡时D的物质的量应大于0.5mol,故m>0.5,故C正确;0.122mol•L-1 0.078mol•L-1×0.078mol•L-1
D、将Ⅲ与I比较,转化率减小,平衡向逆向移动,K减小,如反应放热,可升温,如反应吸热,可降温,因无反应速率大小的比较,故无法判断,故D错误.
故选C.
