问题
选择题
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2  2Cl2+2H2O
2Cl2+2H2O
已知:Ⅰ、反应A中,4mol HCI被氧化,放出115.6kJ的热量。
Ⅱ、
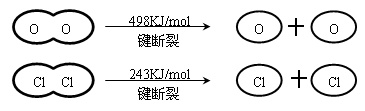
判断下列说法正确的是
A.反应A的△H >-115.6 kJ·mol-1
B.H2O中H—O 键比HCl中H—Cl键弱
C.由Ⅱ中的数据判断氯元素的非金属性比氧元素强
D.断开1 mol H—O 键与断开 1 mol H—Cl 键所需能量相差约为32kJ
答案
答案:D
题目分析:反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以有4x+498kJ-2×243kJ-2×2×y=-115.6kJ,解得y-x=31.9,所以选项D正确,A和B不正确。键能大小不能作为判断氯元素和氧元素非金属性强弱的依据,C不正确,答案选D。
点评:该题是中等难度的试题,试题设计新颖,基础性强。该题的关键是明确从微观的角度去理解反应热的计算,有利于培养学生严谨的逻辑思维能力和发散思维能力,以及灵活运用基础知识解决实际问题的能力。