问题
填空题
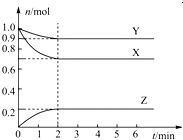
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
(1)该反应的化学方程式为______;
(2)反应开始至2min,用气体Z表示的反应速率为______;
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的______倍;
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为______反应(填“放热”或“吸热”).
答案
(1)△n(X)=0.3mol;△n(Y)=0.1mol;△n(Z)=0.2mol,所以三者计量数之比为3:1:2,故答案为:3X+Y⇌2Z;
(2)v(Z)=
=△c △t
=△n V•△t
=0.05mol•L-1•min-1,故答案为:0.05mol•L-1•min-1; 0.2mol 2L•2min
(3)①根据图象中可知,开始时气体总物质的量为:2mol;平衡后气体总物质的量为:0.9mol+0.7mol+0.2mol=1.8mol;
=P平衡 P起始
=n平衡 n起始
=0.9,1.8mol 2mol
故答案为:0.9;
②压强变大,平衡向右移动,而体系温度降低,说明正反应方向为吸热,故答案为:吸热.
