由氢气和氧气反应生成1mol水蒸气放热241.8KJ。
(1)写出该反应的热化学方程式_______________________ 。
(2)若1g水蒸气转化成液态水时放热2.444KJ,则反应H2(g) + 1/2O2(g) == H2O(l)的
△H=______________ kJ·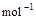 。
。
( 4分)(1) H2(g) + 1/2O2(g) == H2O(g) △H=-241.8 kJ·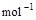 (2)-285.8
(2)-285.8
题目分析:(1)氢气和氧气反应生成1mol水蒸气放热241.8KJ,所以该反应的热化学方程式是H2(g) + 1/2O2(g) == H2O(g) △H=-241.8 kJ·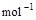 。
。
(2)若1g水蒸气转化成液态水时放热2.444KJ,则18g水蒸气转化成液态水时放热2.444KJ×18=43.992kJ,所以反应H2(g) + 1/2O2(g) == H2O(l)的△H=(-241.8-43.992)kJ/mol=-285.8 kJ/mol。
点评:该题是基础性试题的考查,也是高考中的常见题型,难度不大。该题的关键是明确热化学方程式的含义以及书写的注意事项,然后灵活运用即可。有利于培养学生的规范答题能力。
