问题
计算题
在一定条件下将物质的量相等的NO和O2混合发生如下反应:2NO+O2 2NO2,2NO2
2NO2,2NO2 N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
N2O4。所得混合气体中NO2的体积分数为40%,混合气体的平均相对分子质量。
答案
49.6
设起始NO物质的量为x:
2NO+O2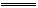 2NO2 则剩余O2的体积为:
2NO2 则剩余O2的体积为:
2 1 2
x x/2 x VO2=x/2mol
设生成的NO2有ymol转化成N2O4
2NO2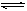 N2O4
N2O4
起始物质的量 x 0
转化物质的量 2y y
平衡物质的量 x-2y y
混合气体总物质的量为
n总=x-2y+y+(x/2)=x+(x/2)-y
依题意有:(x-2y/x+(x/2)-y)=(40/100)
解得x=4y
∴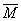 =(32×(x/2)+46(x-2y)+92×y/x+x/2-y)
=(32×(x/2)+46(x-2y)+92×y/x+x/2-y)
=(64y+184y/5y)=49.6
