问题
计算题
在一定温度下将100mLN2,H2混合气充入密闭恒压容器内,发生反应达到平衡时维持温度不变,测得混合气的密度是反应前密度的1.25倍,平均分子量为15.5。求平衡时N2的转化率;N2,H2两种气体开始时各为多少毫升?
答案
平衡时N2的转化率25%;N2,H2两种气体开始的体积分别为40mL和60mL。
∵同T同P下有(ρ1/ρ2)=(m1/m2)
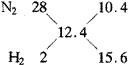
∴有(1/1.25)=(m1/15.5)解得m1=12.4
(V1/V2)=(n1/n2)
即:VN2∶VH2=10.4∶15.6
∴VN2=10.4/(10.4+15.6)×100mL=40mL
VH2=100mL-40mL=60mL
设N2转化的体积为x,则有:
N2 + 3H2 2NH3
2NH3
起始体积 40 60 0
转化体积 x 3x 2x
平衡体积 40-x 60-3x 2x
V总=40-x+60-3x+2x=100-2x
∴有:
15.5=((40-x)×28+(60-3x)×2+2x×17)/(100-2x)
解得x=10mL
∴N2的转化率为:
N2%=(10/40)×100%=25%
