下列有关热化学方程式或反应热的说法正确的是( )
A.已知:H2(g)+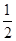 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则H2的燃烧热为-241.8 kJ·mol-1
B.已知:S(g)+O2(g)=SO2(g) ΔH1=-Q1;S(s)+O2(g)=SO2(g) ΔH2=-Q2(Q1、Q2均正值),则Q1<Q2
C.已知: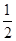 H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=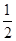 Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2|
Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2|
D.已知:Fe2O3(s)+3C(石墨,s)=2Fe(s)+3CO(g) ΔH=+489.0 kJ·mol-1;CO(g)+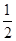 O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1
O2(g)=CO2(g)ΔH=-283.0 kJ·mol-1;C(石墨,s)+O2(g)=CO2(g)ΔH=-393.5 kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s) ΔH=-1641 kJ·mol-1
答案:D
注意题给方程式中水的状态为气态,而H2的燃烧热是指1 mol H2完全燃烧生成液态水时的反应热,A项错误;气态硫变为固态硫时要放热,故等量的硫燃烧时,气态硫放热多,Q2<Q1,B项错误;浓硫酸溶于水放热,弱电解质CH3COOH和NH3·H2O电离要吸热,故浓硫酸与NaOH反应放出的热量较多,|ΔH2|<|ΔH1|,C项错误;根据盖斯定律计算,可知D项正确。
点拨:本题考查反应热知识,意在考查考生的分析、判断能力。