已知以下信息:在浓硫酸中存在平衡:H2SO4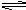 H++HSO4- HSO4-
H++HSO4- HSO4-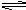 H++SO42-;PbSO4难溶于水和HNO3,但能溶于浓硫酸和醋酸铵溶液。请回答下列有关问题:
H++SO42-;PbSO4难溶于水和HNO3,但能溶于浓硫酸和醋酸铵溶液。请回答下列有关问题:
(1)在试管中加入少许PbSO4并加入数毫升水,震荡得悬浊液,往该悬浊液中加入适量醋酸铵固体,震荡后得到澄清溶液,该反应发生的原因可能是 。请写出该反应的离子方程式: ;
(2)往该澄清溶液中通入H2S气体,有黑色沉淀(PbS)生成,请写出该反应的化学方程式: 。
(3)由上面的实验推测,PbSO4和PbS的溶解度 大。
(4)将少量PbSO4粉末投入盛浓硫酸的试管,震荡后也得澄清溶液,请结合平衡移动原理解释PbSO4能溶于浓硫酸的原因 。
(1)(CH3COO)2Pb是难电离的物质;PbSO4+2 CH3COO - (CH3COO)2Pb+SO42-
(CH3COO)2Pb+SO42-
(2)(CH3COO)2Pb+H2S=PbS↓+2CH3COOH
(3)PbSO4
(4)将PbSO4投入浓硫酸中,浓硫酸中H+结合SO42-生成HSO4-,导致平衡PbSO4(s)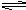 Pb2+(aq)+ SO42-(aq)向右移动,因此,PbSO4能溶于浓硫酸。
Pb2+(aq)+ SO42-(aq)向右移动,因此,PbSO4能溶于浓硫酸。
本题主要考查学生分析问题和解决问题的能力。PbSO4的悬浊液中加入醋酸得澄清溶液,根据化合价规则,二者不发生氧化还原反应,则必发生复分解反应,故只能是生成物中有难电离的物质,只能是醋酸铅了。通入硫化氢则能得到硫化铅沉淀,即相当于在硫酸根离子、硫离子和铅离子同时存在时,硫化铅先沉淀,故硫化铅的溶解度更小。
