问题
选择题
下列说法不正确的是
A.已知H2(g)+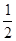 O2(g)===H2O(g) ΔH1=a kJ·mol-1;
O2(g)===H2O(g) ΔH1=a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b
B.CO的燃烧热为283.0 kJ·mol-1,则
2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1
答案
答案:D
选项A中a和b均为负值,因此a>b,A正确;选项B根据燃烧热的定义判断是正确的;由于可逆反应中的反应热表示反应完全进行时的热效应,而合成氨反应是典型的可逆反应,故C正确;根据中和热的定义可知选项D中两反应的中和热是相等的,故D错。
