(14 分) 一氧化碳被广泛应用于冶金工业和电子工业。
⑴高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H="a" kJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H="b" kJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H= kJ·mol-1(用含a、b 的代数式表示)。
⑵电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g) HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g) CH3OH(g) +CO(g) △H>0
CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:
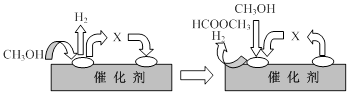
图中中间产物X的结构简式为 。
②在工业生产中,为提高CO的产率,可采取的合理措施有 。
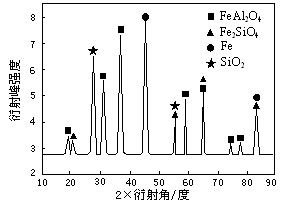
⑶为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为 。
⑷某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。
上述两步中消耗CO的物质的量之比为 。
⑸为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为 。
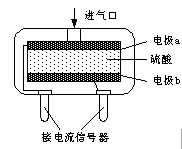
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为 。
⑴(2a+b)/3 ⑵①HCHO ②升高温度,降低压强
⑶FeAl2O4+8H+=Fe2++2Al3++4H2O ⑷3:8
⑸①0.1mol(或0.1NA) ②CO+H2O-2e-=CO2+2H+(每空2分,共14分)
题目分析:⑴将“①×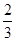 +②×
+②×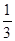 ”能得该方程式,根据盖斯定律可该反应热△H=(2a+b)/3 kJ·mol-1。
”能得该方程式,根据盖斯定律可该反应热△H=(2a+b)/3 kJ·mol-1。
⑵①CH3OH脱氢后生成HCHO;
②根据第一步和第二步的反应特点,可知“升高温度,降低压强”能提高CO的产率;
⑶根据“反应后混合物中的一种产物能与盐酸反应生产两种盐”说明该反应的反应物有FeAl2O4、盐酸,生成物有FeCl2、AlCl3、H2O,据此便可写出离子方程式。
⑷先确定发生的两步反应:3CO+Ni2O3=3CO2+2Ni,Ni+4CO=Ni(CO)4,则这两步中消耗CO的物质的量之比为3:8。
⑸①根据“PdCl2~Pd~2e-”,则每生成5.3gPd沉淀,反应转移电子数为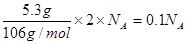 。
。
②CO在负极上发生氧化反应,据得失电子守恒有CO-2e―――CO2,再据电荷守恒有CO-2e――CO2+2H+,最后据原子守恒得CO+H2O-2e-=CO2+2H+。
