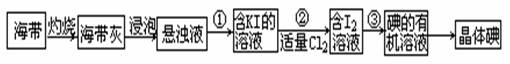
(10分)化学在生活中有很多的应用,如臭氧可用于空气净化、饮用水消毒、工业废物处理和作为漂白剂等,氮化硅(Si3N4)是一种新型陶瓷材料,具有较高的硬度且耐高温。
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。已知: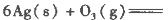
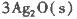 反应生成3 mol Ag2O(s)时放出的热量为
反应生成3 mol Ag2O(s)时放出的热量为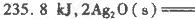
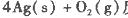 反应生成4 mol Ag(s)时吸收的热量为62.2 kJ,试根据题给数据判断O3转化为O2是________(填“放热”或“吸热”)反应。
反应生成4 mol Ag(s)时吸收的热量为62.2 kJ,试根据题给数据判断O3转化为O2是________(填“放热”或“吸热”)反应。
(2)氮化硅()可由石英与焦炭在高温的氯气流中通过如下反应制得:
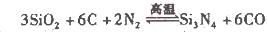
在VL的密闭容器中进行反应,实验数据如下表:
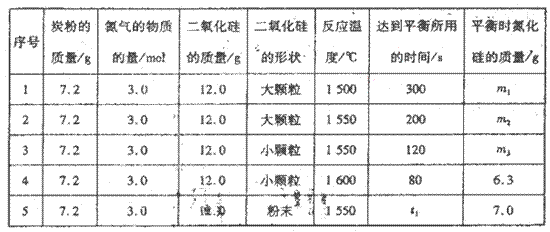
①实验l和实验2表明,________对反应速率有影响,对同一规律研究的实验还有一组是________(填实验序号)。本实验还研究了_______对反应速率的影响。。
②实验5中,t1________(填“>”、“<”或“=”)120,平衡时,二氧化硅的转化率为____________________。
(1)放热
(2)①温度;实验3和实验4;反应物的形状;
②<;41.7%
题目分析:(1)根据题目所给信息,结合盖斯定律判断臭氧转化为氧气2O3(g)=3O2(g)的△H=-235.8 kJ/mol×2+62.2 kJ/mol×3=-285kJ/mol<0,所以该反应是放热反应;
(2)① 实验l和实验2的不同之处在于温度的不同,所以实验l和实验2表明温度对反应速率有影响;对同一规律研究的实验还有一组是实验3和实验4,只是温度不同,其他均相同;通过分析表中数据,其他条件相同而二氧化硅的形状不同,反应速率也不同,所以本实验还研究了反应物的形状对反应速率的影响;
②实验5与实验3相比,只是二氧化硅的形状不同,其余条件均相同,反应物的表面积越大,反应速率越快,粉末状比小颗粒的表面积大,所以t1<120;二氧化硅的初始量是12.0g,平衡时的质量是7.0g,所以消耗5.0g,二氧化硅的转化率是5.0g/12.0g×100%=41.7%。