某温度下,反应 2CH3OH(g) 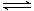 CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
A.CH3OH的起始浓度为1.04 mol/L
B.此时逆反应速率大于正反应速率
C.平衡时,CH3OH的浓度为0.04 mol/L
D.平衡时,CH3OH的转化率小于80%
答案:C
由表格中数据可求得甲醇的起始浓度为
反应 2CH3OH(g)  CH3OCH3(g) + H2O(g)
CH3OCH3(g) + H2O(g)
起始浓度: 1.64 0 0
转化浓度: 1.2 0.6 0.6
该时刻浓度:0.44 0.6 0.6
平衡时:
由表格所给数据可求得: =
= <400,故反应将正向进行,正反应速率大于逆反应速率;
<400,故反应将正向进行,正反应速率大于逆反应速率;
而平衡时各物质浓度:
反应 2CH3OH(g)  CH3OCH3(g) + H2O(g)
CH3OCH3(g) + H2O(g)
起始浓度: 1.64 0 0
转化浓度: x x/2 x/2
平衡时: 1.64-x x/2 x/2
代入平衡常数关系式可求得:K= =400,得x为1.6 mol/L,故平衡时CH3OH的浓度为0.04 mol/L,其转化率为
=400,得x为1.6 mol/L,故平衡时CH3OH的浓度为0.04 mol/L,其转化率为 >80%
>80%
故答案为C
