问题
选择题
已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625kJ·g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H =-890kJ/mol
B.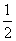 CH4(g)+O2(g)=
CH4(g)+O2(g)=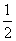 CO2(g)+H2O(l);△H=-445kJ/mol
CO2(g)+H2O(l);△H=-445kJ/mol
C.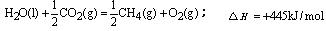
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-55.625kJ/mol
答案
答案:D
题目中给出的数据意义是:燃烧1g的甲烷放出55.625kJ的热量,应该换算成燃烧1mol甲烷放出的热量为890kJ。热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ·mol-1其他系数与热量相对应的方程式均正确。
