问题
选择题
一定条件下,在容积为10L的密闭容器中,将l mol X和1 mol Y进行如下反应:2X(g)+Y(g) 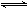 Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是
Z(g),经60 s达到平衡生成0.3 mol的Z,下列说法正确的是
A.60 s时Z的平衡浓度为0.03 mol/L
B.将容器容积变为20 L,Z的新平衡浓度将等于原平衡浓度的一半
C.若温度和体积不变,往容器内增加1 mol N2,压强增大,Y的转化率将增大
D.若升高温度,X的体积分数增大,则正反应的△H>0
答案
答案:A
2X(g)+Y(g) 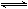 Z(g)
Z(g)
起始量(mol) 1 1 0
转化量(mol) 0.6 0.3 0.3
平衡量(mol) 0.4 0.7 0.3
保持温度和体积不变,增加X的浓度,可以提高其它反应物的转化率,但自身转化率会降低。因为反应是体积减小的可逆反应,当容器体积变为20L时,体系内压强降低,平衡向逆反应方向移动,所以Z的新平衡浓度将小于原平衡浓度的1/2。升高温度,X的体积分数增大,说明平衡向逆反应方向移动,因此正反应是放热反应。所以正确的答案是A。
