将6mol A和5mol B两气体通入容积为4L的密闭容器,一定条件下反应:3A(气)+B(气) 2C(气)+xD(气)+Q经5min达平衡,此时生成2mol C,测得D的平均反应速率为0.1mol·(L·min)-1,下列说法中正确的是
2C(气)+xD(气)+Q经5min达平衡,此时生成2mol C,测得D的平均反应速率为0.1mol·(L·min)-1,下列说法中正确的是
A.若降低该平衡体系的温度,则逆反应速率减小,正反应速率增大
B.恒温下,当容器中C和D的生成速率达到相等时,该反应达到平衡状态
C.A的平均反应速率为0.15mol·(L·min)-1
D.达平衡时B的转化率为25%
答案:C
分析:A、降低温度,正逆反应速率都降低,该反应为放热反应,逆反应速率降低快,正反应速率降低慢,平衡向正反应移动;
B、可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
C、根据C的物质的量,利用v= 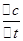 计算v(C),再利用速率之比等于化学计量数之比计算v(A);
计算v(C),再利用速率之比等于化学计量数之比计算v(A);
D、根据C的物质的量,利用方程式计算出参加反应的B的物质的量,再利用转化率定义计算.
解:A、降低温度,正逆反应速率都降低,该反应为放热反应,逆反应速率降低快,正反应速率降低慢,平衡向正反应移动,故A错误;
B、C和D的生成速率都表示正反应速率,二者相等,不能说明反应达到平衡,故B错误;
C、v(C)=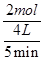 =0.1mol/(L?min),v(A)=
=0.1mol/(L?min),v(A)=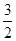 v(C)=
v(C)=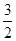 ×0.1mol/(L?min)=0.15mol/(L?min),故C正确;
×0.1mol/(L?min)=0.15mol/(L?min),故C正确;
D、对于反应3A(g)+B(g) 2C(g)+xD(g),
2C(g)+xD(g),
起始:5mol 0
转化:1mol 2mol
所以B的转化率为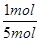 ×100%=20%,故D错误.
×100%=20%,故D错误.
故选C.
