问题
选择题
已知N2(g)+3H2(g) 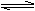 2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是
2NH3(g),现向一密闭容器中充入1molN2和3molH2,在高温、高压和催化剂存在条件下发生反应。下列有关说法正确的是
A.最终可以生成2mol NH3
B.达到化学平衡状态时,正反应和逆反应的速率都为0
C.达到化学平衡状态时,容器中N2、H2和NH3的物质的量之比为1∶3∶2
D.达到化学平衡状态时,N2、H2和NH3的物质的量浓度不再变化
答案
答案:D
分析:可逆反应不能进行彻底,当达到化学平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不再发生变化,注意反应方程式的前后计量数关系.
解:A.反应为可逆反应,反应物不能完全转化,故A错误;
B.达到化学平衡状态时,正反应和逆反应相等但不为0,故B错误;
C.反应的外界条件不确定,反应物的转化率不确定,则不能确定平衡时各物质的物质的量关系,故C错误;
D.当达到化学平衡状态时,各物质的浓度不再改变,故D正确.
故选D.
