问题
选择题
某体积可变的密闭容器中盛有适量的N2和H2的混合气体,在一定条件下发生反应:N2(g)+3 H2(g) 2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中NH3的体积是0.1 V L。
2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中NH3的体积是0.1 V L。
A.原混合气体的体积为1.2V L
B.原混合气体的体积为1.1VL
C.反应达平衡时N2消耗掉0.05 V L
D.反应达平衡时H2消耗掉0.5 V L
答案
答案:B
N2(g)+3 H2(g)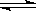 2NH3(g)
2NH3(g)
反应前:X Y 0
转化: 0.05V 0.15V 0.1V
平衡: X-0.05V Y-0.15V 0.1V
根据方程式可知:生成多少体积的氨气,总体积就减少多少,所以,原混合气体的体积为V L+0.1 V L=1.1VL,选项A错误,B正确。C 正确,D 错误,反应达平衡时H2消耗掉0.15 V L,故选BC
