问题
选择题
在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3 (g)+ Q,其平衡常数K与温度T的关系如下表:
2NH3 (g)+ Q,其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②如果合成氨反应的方程式写为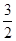 N2(g)+
N2(g)+ 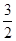 H2(g)
H2(g) NH3(g),其平衡常数为K’,则K’与K的关系为K’ = 。
NH3(g),其平衡常数为K’,则K’与K的关系为K’ = 。
答案
>; 。(2分)
。(2分)
①合成氨的反应为放热反应,随温度升高平衡向逆反应方向移动,即K减小;所以K1> K2;
②平衡常数指可逆反应达到平衡后生成物浓度幂之积与反应物浓度幂之积的比值,所以,当方程式的化学计量数减半后,其平衡常数将为原来的 ,即K’=
,即K’=
